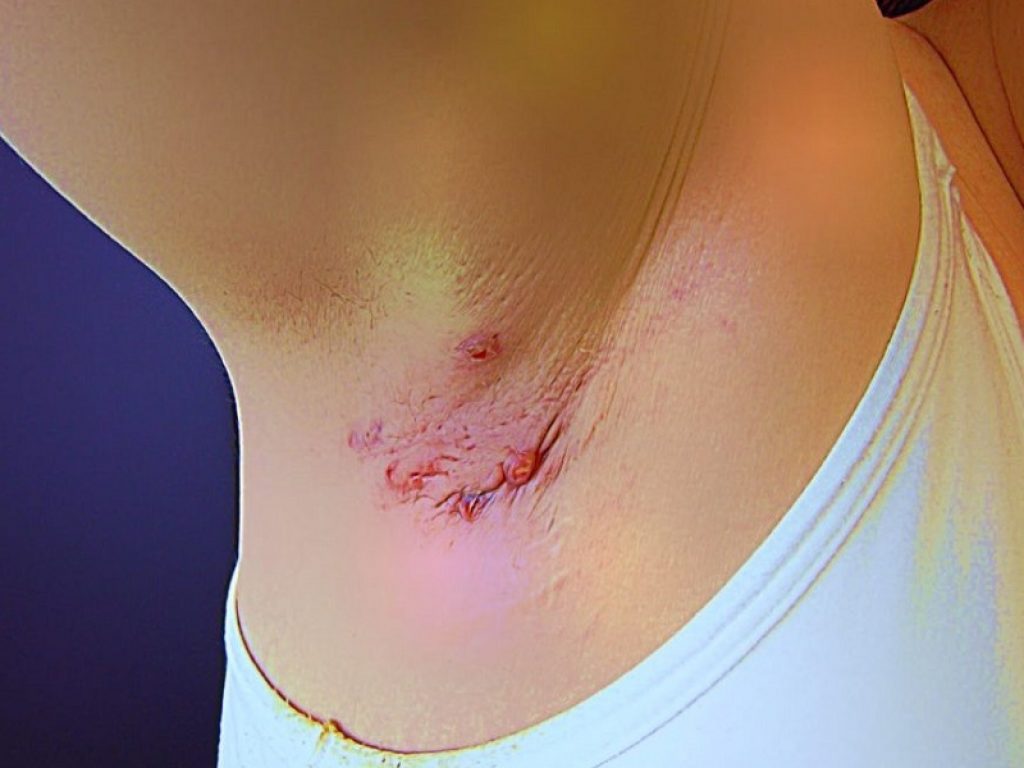
Idrosadenite suppurativa: arrivano risultati promettenti in fase III per il farmaco sperimentale izokibep
Nelle persone affette da idrosadenite suppurativa da moderata a grave il trattamento con l’inibitore sperimentale dell’interleuchina-17A izokibep induce risposte cliniche entro poche settimane di trattamento, secondo i risultati di uno studio randomizzato e controllato di fase III presentato al congresso della European Academy of Dermatology and Venereology (EADV) 2024.
L’idrosadenite suppurativa influenza notevolmente la qualità della vita delle persone che ne sono affette, pertanto siamo costantemente alla ricerca di terapie nuove e più efficaci, ha fatto presente il relatore Kim Papp, di Probity Medical Research, a Waterloo, Ontario, Canada.
Un candidato promettente è izokibep, un inibitore sperimentale dell’interleuchina-17A, considerato una piccola proteina terapeutica a causa delle sue dimensioni di soli 18,6 kDa, circa un decimo di quelle di un anticorpo monoclonale standard. Il farmaco è progettato per inibire selettivamente la citochina con elevata potenza e contiene un dominio che si lega all’albumina.
«Il legame con l’albumina è importante perché estende l’emivita del farmaco e consente a izokibep di essere trasportato o mobilizzato nei tessuti bersaglio» ha spiegato. «Quindi, con un vantaggio teorico di una maggiore penetrazione nei tessuti bersaglio rispetto ad altri inibitori della IL-17A a molecole più grandi, l’obiettivo di questo studio era valutare se questa peculiarità rappresentasse un vantaggio in termini di efficacia e sicurezza nelle persone con idrosadenite da moderata a grave.
Valutazione dell’efficacia e della sicurezza di izokibep vs placebo
Lo studio di fase III presentato al congresso, randomizzato, in doppio cieco, controllato con placebo, ha coinvolto soggetti con idrosadenite suppurativa diagnosticata da almeno 6 mesi, con lesioni di stadio Hurley II o III in almeno 2 aree anatomiche distinte, un conteggio totale di almeno 5 ascessi e noduli infiammatori (AN) e una risposta inadeguata, intolleranza o controindicazione agli antibiotici orali.
In totale 258 partecipanti sono stati randomizzati in rapporto 1:1 a ricevere un’iniezione sottocutanea di izokibep una volta alla settimana alla dose di 160 mg oppure placebo corrispondente.
«Il progetto iniziale dello studio era di 16 settimane, sulla base delle analisi molto precoci eseguite in un trial precedente» ha osservato Papp. «Tuttavia immaginavamo che i risultati ottimali sarebbero effettivamente stati raggiunti prima, quindi gli endpoint primari in questo studio sono stati spostati a 12 settimane».
Le caratteristiche basali erano ben abbinate tra i gruppi. Nel complesso l’età media dei partecipanti era di 37 anni, il 69% erano donne, il 70% erano bianchi, il 19% neri o afroamericani, il 7% asiatici e il 4% erano raggruppati come altra etnia. L’indice di massa corporea medio (BMI) era 34, il 43% erano fumatori abituali e la durata media della malattia era di 10,2 anni. Il conteggio medio di AN era 12,4 e il numero medio di tunnel drenanti era 2,2.
Riduzione significativa della gravità dell’idrosadenite vs placebo
Un terzo dei pazienti in trattamento attivo ha ottenuto una riduzione di almeno il 75% nel punteggio Hidradenitis Suppurativa Clinical Response (HiSCR 75) a 12 settimane, l’endpoint primario dello studio, in confronto al 21% del gruppo placebo (P<0,05).
Anche le percentuali dei soggetti con risposta HiSCR 90/100 erano significativamente più elevate nel gruppo izokibep in confronto al gruppo placebo, rispettivamente izokibep 25% e 22% vs placebo 9% e 8%, tuttavia la risposta HiSCR 50 è stata raggiunta da quote simili di partecipanti nei due gruppi (48% per izokibep e 37% per il placebo), con una differenza non significativa.
«Nello studio, anche se l’endpoint primario è stato raggiunto, sono stati osservati tassi di risposta al placebo elevati» ha commentato Hans Christian Ring, dermatologo del Bispebjerg Hospital di Copenaghen, in Danimarca. «Tuttavia un dato simile si è verificato anche in altri studi recenti con diversi anticorpi monoclonali, un risultato che potrebbe riflettere i limiti del parametro HiSCR per valutare la risposta alla terapia e la complessità patogena della malattia».
Miglioramenti anche in altri spetti della patologia
Anche il dolore cutaneo, la qualità della vita e i conteggi AN sono migliorati significativamente con il trattamento con izokibep rispetto al placebo a 12 settimane, anche se non è stata osservata una differenza nelle riacutizzazioni della malattia:
- Una riduzione di almeno tre punti nella scala di valutazione numerica per il dolore cutaneo è stata ottenuta nel 33% del gruppo attivo rispetto al 17% con il placebo (P<0,05).
- I punteggi del Dermatology Life Quality Index sono stati ridotti in media di 4,9 punti a 12 settimane a partire da un valore basale di 12,3 nel gruppo izokibep e in media di 2,7 da un valore basale di 11,4 nel gruppo placebo (P<0,01).
- Un conteggio AN di 0, 1 o 2 è stato ottenuto nel 50% dei soggetti trattati con izokibep rispetto al 27% di quelli trattati con placebo (P<0,01).
- Le riacutizzazioni di idrosadenite si sono invece verificate in una percentuale simile di pazienti (29% con izokibep vs 31% con il placebo.
Eventi avversi emergenti dal trattamento sono stati registrati in un maggior numero di pazienti sottoposti a izokibep rispetto al placebo (79% vs 53%) con le reazioni al sito di iniezione come i più frequenti (rispettivamente 65% vs 8%), causa di interruzione della terapia rispettivamente nel 5% e nello 0% dei pazienti.
In entrambi i gruppi è stata segnalata cefalea in circa il 10% dei partecipanti e rinofaringite nel 7%. Stanchezza e diarrea sono state registrate più spesso nel gruppo izokibep (5,4% per entrambi) rispetto al gruppo placebo (2,3% per stanchezza e 1,6% per diarrea).
Hanno completato le 12 settimane di trattamento circa l’81% dei soggetti assegnati a izokibep e l’87% del gruppo placebo, prevalentemente per ritiro del consenso e perdita al follow-up, piuttosto che a causa di problemi di sicurezza.
Ring ha considerato incoraggiante il fatto che non siano stati osservati casi di infezioni da candida o malattia infiammatoria intestinale, «tuttavia è sorprendente che il 65% dei pazienti abbia manifestato reazioni nel sito di iniezione, una frequenza notevolmente più alta rispetto ad altre terapie biologiche comparabili» ha affermato. «Inoltre è stato segnalato un numero elevato cefalee, che potenzialmente potrebbe portare alla sospensione del trattamento.»
Referenze
Papp KA et al. Efficacy and safety of izokibep, a novel IL-17A inhibitor, in moderate-to-severe hidradenitis suppurativa: Week 12 results from a randomized, double-blind, placebo-controlled, multicenter, phase 3 study. Presented at the 33rd Annual Congress of the European Academy of Dermatology & Venereology (EADV); Amsterdam, Netherlands; September 25–28, 2024.